Coulter Electronics (1976 - 2009)
Series Epics V y 750 - 1979 a 1985
Una serie de instrumentos que eran esencialmente instrumentos láser de iones de argón de 5 W que contaban con un sistema de análisis de datos multiparamétrico, una unidad flexible y una impresora gráfica
|
EPICS V
Solicitud de patente original de 1953 de Coulter |
Láser dual EPICS V
Borradores de publicidad dibujados a mano del primer contador Coulter (1956) |
|
EPICS 541
Solicitud de patente original de 1953 de Coulter |
EPICS 750
Borradores de publicidad dibujados a mano del primer contador Coulter (1956) |
Stuart Schlossman
- Schlossman, del Instituto Farber de Boston, comenzó a fabricar anticuerpos monoclonales contra antígenos de glóbulos blancos en 1978. Finalmente colaboró con Ortho Diagnostics, que distribuyó los famosos mAbs (anticuerpos monoclonales) "OK T4", etc., Mabs
- Coulter Immunology también adquirió los derechos sobre sus anticuerpos
Historia de Coulter Hematology
Modelo A de 1953

Células medidas electrónicamente
Modelo S de 1968

CBC completamente automatizado
S Plus de 1977

CBC completamente automatizado
VC de 1985

Integración de la citometría de flujo en un analizador hematológico
Celda Gen•S de 2000

- AccuFlex
- Reglas de apoyo a las decisiones
- IntelliKinetics
- Reticulocitos automatizados
- SlideMaker y SlideStainer integrados
VC de 1985
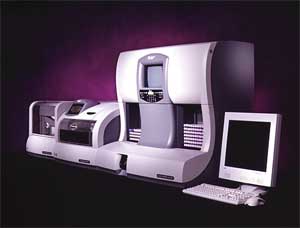
- Acceso aleatorio
- Tecnología AccuCount
- Linealidad extendida
- Menos necesidad de intervención manual
- Corrección de interferencia WBC
- Enumeración NRBC
Historia de la citometría de flujo de Coulter
TPS de 1975

Clasificación de células de dos parámetros
Epics C de 1984

Clasificador de flujo clínico
Epics PROFILE de 1986
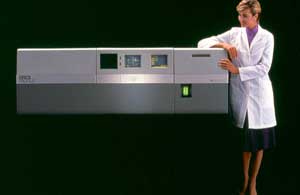
Analizador de flujo clínico
Q Prep de 1987

Preparación automatizada de muestras
Anticuerpos monoclonales Cyto-Stat de 1988

- Listo para usar
- Sin lavado
- Anticuerpos de uno y varios colores
EPICS XL / XL-MCL de 1993

- Analizador de sobremesa
- Análisis de cuatro colores
- Cargador automático de muestras
- Procesamiento de señales digitales
Citómetros de flujo
Los citómetros de flujo modernos pueden analizar varios miles de partículas por segundo, en "tiempo real", y pueden separar y aislar de forma activa las partículas con propiedades específicas. Un citómetro de flujo es similar a un microscopio, excepto que, en lugar de producir una imagen de la célula, la citometría de flujo ofrece una cuantificación automatizada "de alto rendimiento" (para un gran número de células) de los parámetros establecidos. Para analizar tejidos sólidos, primero se debe preparar la suspensión de una sola célula.
Los primeros citómetros de flujo fueron, en general, dispositivos experimentales, pero los recientes avances tecnológicos han creado un mercado considerable para la instrumentación, así como para los reactivos utilizados en el análisis, como los anticuerpos marcados con fluorescencia y el software de análisis. Los instrumentos modernos suelen tener múltiples láseres y detectores de fluorescencia (el máximo actual de un instrumento comercial es de 4 láseres y 18 detectores de fluorescencia).
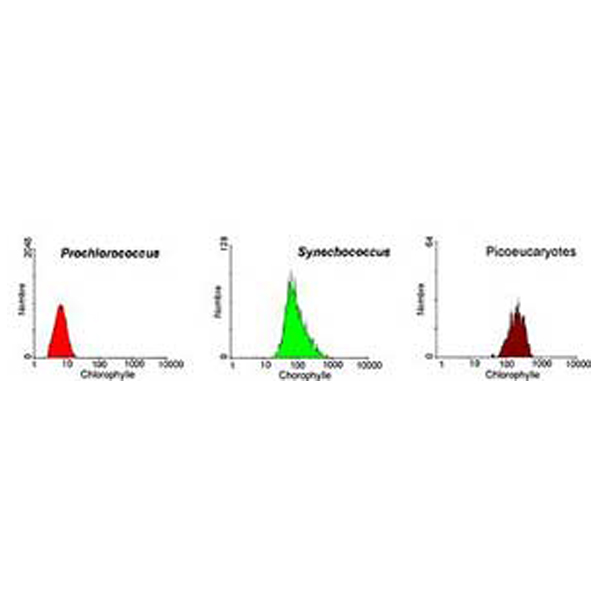 |
Análisis de una muestra marina de picoplancton fotosintético mediante citometría de flujo que muestra tres poblaciones diferentes (proclorococos, sinecocos y picoeucariotas)
El aumento del número de láseres y detectores permite el etiquetado múltiple de anticuerpos y permite identificar con mayor precisión una población objetivo por su fenotipo. Ciertos instrumentos incluso pueden tomar imágenes digitales de células individuales, permitiendo el análisis de la localización de la señal fluorescente dentro de las células o en su superficie. Los datos generados por los citómetros de flujo pueden representarse en una sola dimensión para producir un histograma o en gráficos bidimensionales o incluso tridimensionales. Las regiones de estos gráficos se pueden separar de forma secuencial según la intensidad de la fluorescencia para crear una serie de extracciones de subconjuntos, denominados "ventanas de selección". Existen protocolos de selección específicos para fines clínicos y diagnósticos, especialmente en relación con la hematología. Los gráficos se realizan a menudo en escala logarítmica. Debido a que los diferentes espectros de emisión de los tintes fluorescentes se superponen [1], las señales en los detectores deben ser compensadas tanto de forma electrónica como computacional. A menudo, los datos acumulados con el citómetro de flujo se pueden volver a analizar (utilizando un software, por ejemplo, Kaluza™ [5]) en otro lugar, liberando la máquina para que otras personas la utilicen.
Instrumentos comerciales
La completa gama de sistemas de automatización e información de Beckman Coulter le ayuda a agilizar los procesos para lograr la máxima eficiencia. Desde la entrega de resultados de pruebas de pacientes más oportunos, precisos y fiables hasta la eliminación de cuellos de botella, nuestras soluciones en sistemas de automatización e información le permiten gestionar las operaciones del laboratorio de forma más eficiente y rentable.





